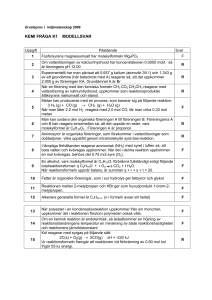
Bildningsentalpi ΔHf0 är entalpiändringen då en kemisk förening bildas utav grundämnen.
ΔHf0 anges i kJ/mol bildat ämne. H kommer från engelskan Heat content.
Bildningsentalpin för grundämnen är lika med 0.
Om vi har en reaktion mellan olika kemiska föreningar där det bildas nya kemiska föreningar, kan
entalpiändringen (ΔH) för reaktionen beräknas med hjälp av de kemiska föreningarnas
bildningsentalpier.
ΔHreaktionen = ∑ ΔHf0 produkterna - ∑ ΔHf0 reaktanterna
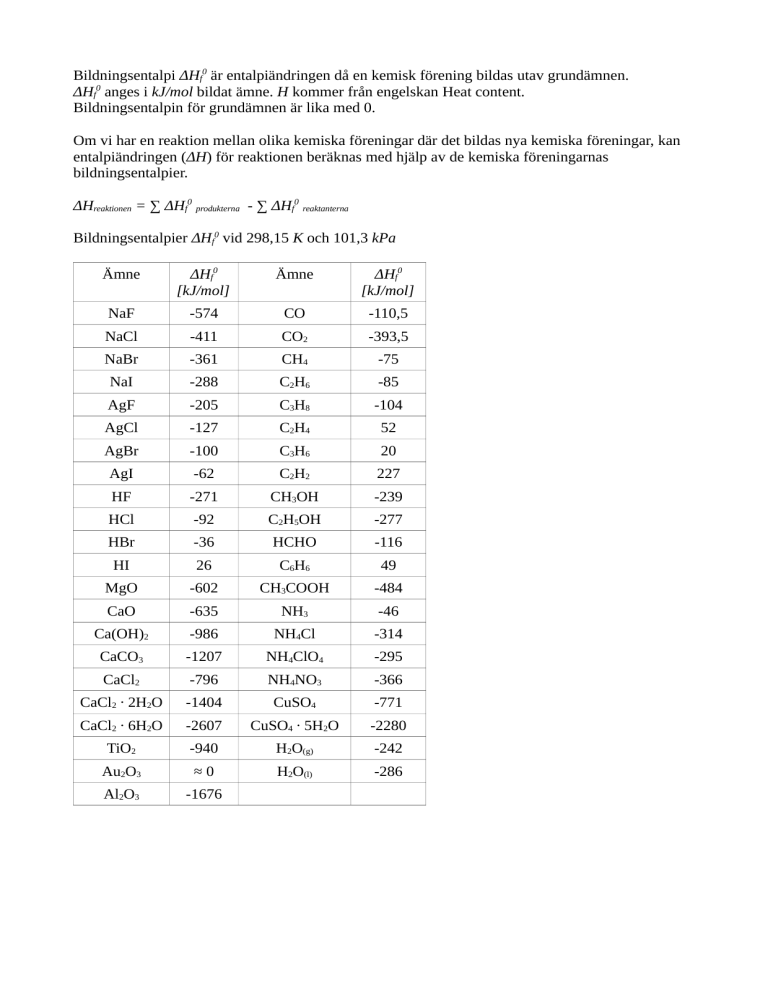
Bildningsentalpier ΔHf0 vid 298,15 K och 101,3 kPa
Ämne
ΔHf0
[kJ/mol]
Ämne
ΔHf0
[kJ/mol]
NaF
-574
CO
-110,5
NaCl
-411
CO2
-393,5
NaBr
-361
CH4
-75
NaI
-288
C2H6
-85
AgF
-205
C3H8
-104
AgCl
-127
C2H4
52
AgBr
-100
C3H6
20
AgI
-62
C2H2
227
HF
-271
CH3OH
-239
HCl
-92
C2H5OH
-277
HBr
-36
HCHO
-116
HI
26
C6H6
49
MgO
-602
CH3COOH
-484
CaO
-635
NH3
-46
Ca(OH)2
-986
NH4Cl
-314
CaCO3
-1207
NH4ClO4
-295
CaCl2
-796
NH4NO3
-366
CaCl2 · 2H2O
-1404
CuSO4
-771
CaCl2 · 6H2O
-2607
CuSO4 · 5H2O
-2280
TiO2
-940
H2O(g)
-242
Au2O3
≈0
H2O(l)
-286
Al2O3
-1676